Kuusi tapaa tosielämän tiedon hyödyntämiseen
Tosielämän tieto kiinnostaa enemmän kuin koskaan aiemmin. Ilmiö ei koske pelkästään Suomea, sillä kiinnostus on maailmanlaajuinen. Alan kasvua todistaa tietopyyntöjen ja tieteellisten julkaisujen lisääntyneet määrät. Tosielämän tiedosta puhutaan paljon, mutta mihin tätä tietoa voidaan hyödyntää?

Edellinen blogitekstini kertoi mitä tosielämän tieto eli RWD ja siitä johdettava tosielämän näyttö eli RWE ovat. Seuraavaksi astun kohti tosielämän tiedon käyttöä.
Tosielämän tietoa voidaan hyödyntää laajasti terveydenhuollon ja lääkekehityksen raamien sisällä. Vähimmillään tuloksista laadittava tieteellinen julkaisu kartuttaa tiedeyhteisön tietämystä, mutta hyvin suunnitellun RWE-tutkimuksen lopputuote on laajasti hyödynnettävissä.
RWE-tutkimus aloitetaan yleensä tietty käyttökohde – kuten lääkkeen korvattavuuden hakeminen – mielessä. RWE-tutkimuksen teko on kuitenkin hidasta. Usein tiedon hyödyntäjän pöydälle tippuu toinenkin ennalta suunnittelematon ja tärkeä käyttökohde juuri tulosten valmistuessa.
Tosielämän tiedon käyttäjiä ovat lääketeollisuus, tiedeyhteisö, viranomaiset, maksajat, potilasjärjestöt, päättäjät, rekisterinpitäjät, lääkärit ja palveluntarjoajat. Viime kädessä hyödyn tosielämän näytöstä saa potilas.
Tämä blogiteksti esittelee kuusi tosielämän tiedon toissijaista käyttöaihetta (kts. ”toisiokäyttö” RWE-sanastosta). Näistä jokainen kokonaisuus pitää sisällään useita yksityiskohtaisempia käyttökohteita. Lista ei ole kaiken kattava, sillä uutta käyttöä RWE:lle keksitään jatkuvasti.
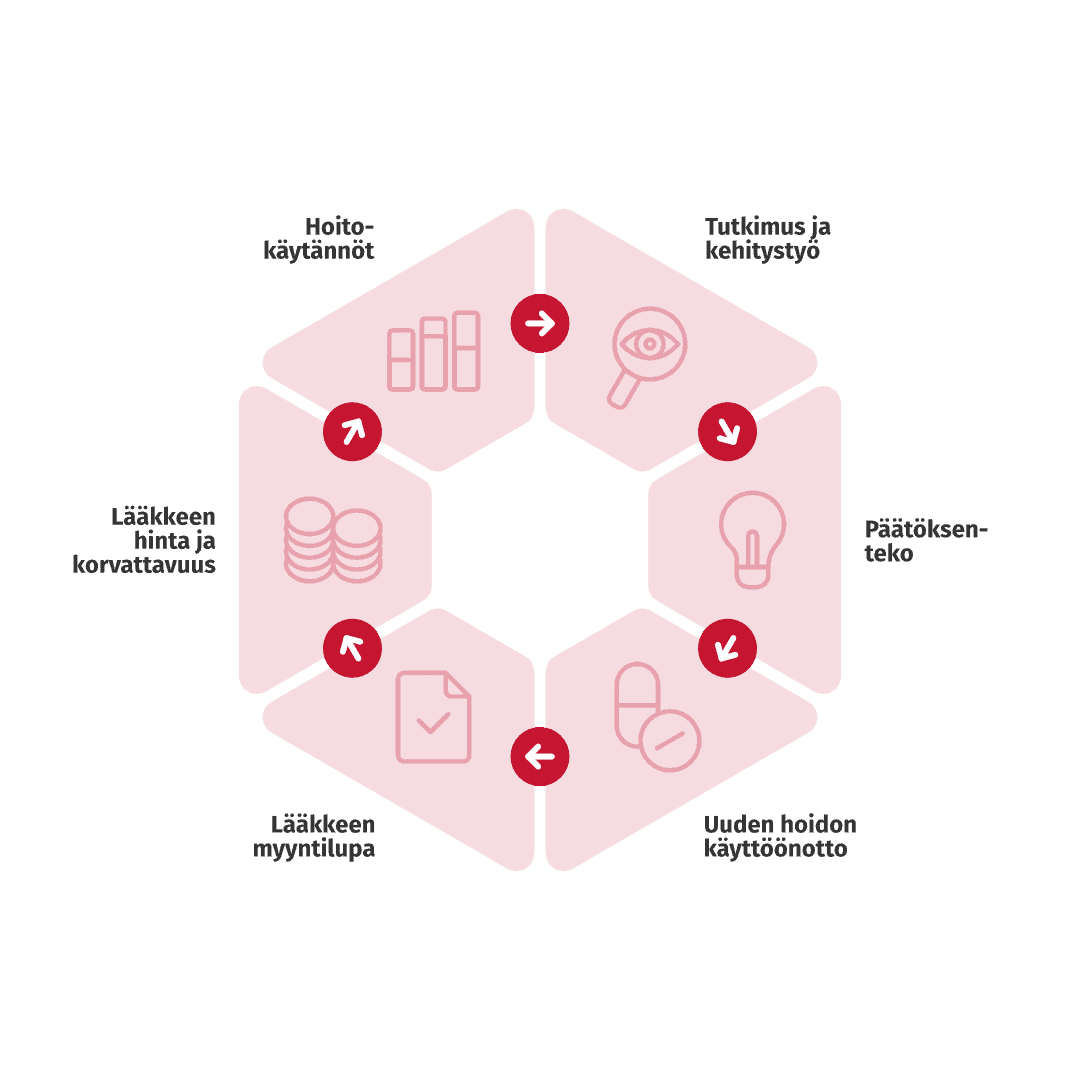
Kuusi tosielämän tiedon toissijaista käyttöaihetta
1. Tutkimus ja kehitystyö
Tosielämän tietoa voidaan käyttää lääkkeen elinkaaren monessa vaiheessa. Uuden lääkemolekyylin tutkimuksen alkaessa käydään läpi aiemmin julkaistua tosielämän näyttöä esimerkiksi tieteellisistä julkaisuista. Perinteisille kliinisille tutkimuksille RWE-tutkimukset tarjoavat esitietoa, täydennystä tai jopa korvaavan vaihtoehdon (kts. ”kliininen tutkimus” RWE-sanastosta). Kliinisiin tutkimuksiin verrattaessa suurempi tutkittavien lukumäärä ilman potilaiden tarkkaa rajausta on RWE-tutkimusten vahvuus. RWE-tutkimuksissa lääkkeen vaikuttavuutta voidaan tarkastella väestötasolla ja pitkän seurannan aikana. COVID-19 on vaikuttanut potilaiden hoitoon, minkä vuoksi pandemian aikana joidenkin kliinisten interventiotutkimusten sijaan on päädytty tekemään RWE-tutkimus. Myös biopankeilla on tärkeä osa tutkimus- ja kehitystyössä, sillä jo olemassa olevan biopankkitiedon lisäksi aineistoja voidaan kehittää analysoimalla potilaiden näytteistä uusia sairauksiin liittyviä markkereita.
2. Päätöksenteko
Terveydenhuoltojärjestelmää, lääkäreitä tai tiettyä potilasryhmää koskevat terveydenhuollon viranomaisten ja maksajien tekemät päätökset pyrkivät kohti kustannustehokasta toimintaa ja lääkkeiden järkevää käyttöä. Tosielämän tietoa voidaan käyttää päätöksenteon tukena ja tiedolla johtamisessa. Vallitseva koronavirustilanne lisää tosielämän tiedon käyttöä entisestään, sillä terveydenhuolto joutuu punnitsemaan resurssien käyttöä entistä tarkemmin. Rekisteritiedon avulla voidaan myös kerätä näyttöä kansallisen rokotusjärjestyksen laatimiselle koronaviruspandemian kaltaisessa tilanteessa. Riskiryhmiä voidaan kartoittaa selvittämällä riskitekijöitä vakavaan COVID-19-tautiin sairastumiselle.
3. Uuden hoidon käyttöönotto
Uuden hoidon käyttöönottoa koskevassa päätöksessä tarvitaan tutkimusnäyttöä hoidon hyödyistä, haitoista, kustannuksista ja kustannusvaikuttavuudesta. Tämän tiedon saa RWE-tutkimuksesta. Ennen uuden lääkkeen käyttöönottoa, voidaan kerätä tietoa lääkkeen kohteena olevasta potilasryhmästä. Toisinaan potilasryhmän koon kansallinen arviointi on haastavaa jopa heitä hoitaville lääkäreille. Tosielämän tieto kuitenkin antaa luotettavan tiedon potilasjoukon koosta. Uutta hoitoa koskevaan kliiniseen lääketutkimukseen voidaan muodostaa verrokkijoukko rekisteripohjaisesti (kts. ”verrokkijoukko” RWE-sanastosta). Kliinisen tutkimuksen potilaille poimitaan heidän kaltaisensa verrokkijoukko rekistereistä. Perinteisestä kliinisestä tutkimuksesta poiketen RWD-verrokkeihin ei kajota millään tavalla.
4. Lääkkeen myyntilupa
Lääkkeen myyntiluvan haltija voi esittää hakemuksensa tukena tosielämän näyttöä potilaspopulaation hoidon kustannuksista ja tehosta verraten perinteistä ja uutta hoitoa. Lääkealaa valvovat viranomaiset ovat erityisen kiinnostuneita keräämään tosielämän tietoa uusien ja innovatiivisten hoitojen kohdalla. Kiinnostus johtuu paitsi näiden hoitojen korkeasta hinnasta niin tutkitun tiedon rajallisuudesta. Tällaisia hoitoja ovat esimerkiksi solu- ja geeniterapiat, kuten CAR-T ja CRISPR.
5. Lääkkeen hinta ja korvattavuus
Lääkkeen hinta- ja korvattavuushakemusta voidaan tukea tosielämän näytöllä. Tietyn potilasryhmän perinteisen hoidon kustannuksia voidaan verrata uuden hoidon kustannuksiin. Lisäksi uuden hoidon paremmuutta voidaan kuvailla tosielämän näytön avulla. Käyttöönoton jälkeen kerättyä näyttöä lääkkeen vaikuttavuudesta voidaan käyttää – tai viranomainen voi sitä jopa vaatia – suositusten tai korvauspäätösten uudelleen arvioinnissa.
6. Hoitokäytännöt
Kun lääke on otettu käyttöön, alkaa toteutuneen käytön tarkastelu rekisteritiedoista. Tällainen tarkastelu saattaa kehittää hoitosuosituksia ja hoitopolkuja tai tuoda lääkkeelle uuden indikaation (kts. ”lääkkeen indikaatio” RWE-sanastosta). Tosielämän tiedosta voidaan tarkastella vastaako toteutunut lääkityksen annostus kliinisen tutkimuksen tai kansallisen suosituksen annostusta ja mikä on toteutuneen hoidon hinta yhteiskunnalle. Myös hoidon tehoa ja turvallisuutta voidaan tarkastella.
Lopuksi
Tosielämän tiedon käyttökohteet ovat moninaiset ja uusia käyttökohteita kehitetään jatkuvasti. Viranomaiset ovat esittäneet toiveen tosielämän näytön käyttämiseksi päätöksenteon tukena. Yhdysvaltain lääke- ja ruokaturvallisuusvirasto FDA aloitti vuonna 2018 strategisen ohjelman RWE:n käytön lisäämiseksi lääkkeiden uusia indikaatioita sekä solu- ja geeniterapioita koskien. Myös Eurooppalaiset viranomaistahot kuten EMA toivoo, että tosielämän näyttöä käytettäisi enemmän päätöksenteon tukena. Tosielämän näytön hyödyntäminen on kuitenkin vielä uutta, eivätkä käyttäjien tietotarpeet ja tiedon hyödyntämismahdollisuudet ole täysin kirkastuneet.
Täysin vakiintuneita käytäntöjä RWE:n käyttöön ei vielä ole, mutta kuljemme parhaillaan sitä kohti. Tehokkain tapa RWE-tutkimuksen hyödyntämiseen löytyy kokemuksen karttuessa ja yhteistyötä tehden.

